- Science:溶瘤病毒联合CAR-T细胞疗法治疗实体瘤取得新进展
- ADC Therapeutics公布靶向CD25 ADC药物Cami治疗实体瘤的临床前研究数据
-
CD37抗体-核素偶联药物Betalutin治疗R/R非霍奇金淋巴瘤1/2a期临床结果积极
- Nature:TRIM37影响细胞分裂的机制与PLK4抑制剂的抗癌潜力
-
NCB:PD-L1在介导肿瘤细胞焦亡和肿瘤坏死过程发挥关键作用
药物开发
Science:溶瘤病毒联合CAR-T细胞疗法治疗实体瘤取得新进展
9月2日,Science Translational Medicine发表了来自希望之城国家医学中心的最新研究。该研究将溶瘤病毒和嵌合抗原受体T细胞(CAR-T)疗法结合在一起,靶向原本难以单独用CAR-T疗法治疗的实体瘤,在临床前研究中获得了积极结果。
研究团队通过基因工程改造了一种溶瘤病毒,使其进入实体瘤细胞,迫使这些肿瘤细胞在表面表达截短的CD19(CD19t)。实验显示,这种溶瘤病毒成功使三阴性乳腺癌细胞系以及胰腺癌、前列腺癌、卵巢癌和头颈癌、脑肿瘤细胞表达CD19t。再通过特异性靶向CD19的CAR-T细胞识别并攻击这些实体瘤细胞,实现CAR-T疗法对实体瘤的治疗。小鼠模型显示利用这种组合疗法根除实体瘤后,小鼠还表现出了长时间的保护性抗肿瘤免疫,免疫系统建立了对肿瘤的记忆反应,说明联合治疗还有助于防止复发。
目前,研究人员正计划在实体瘤患者中测试该种溶瘤病毒的安全性。若证明安全有效,预计将在2022年启动该种溶瘤病毒和CAR-T细胞组合疗法治疗实体瘤患者的临床试验。
(信息来源:
https://stm.sciencemag.org/content/12/559/eaaz1863.full)
ADC Therapeutics公布靶向CD25 ADC药物Cami治疗实体瘤的临床前研究数据
9月10日,Journal for ImmunoTherapy of Cancer在线发表了来自ADC Therapeutics的最新研究。该研究公布了靶向CD25的ADC药物camidanlumab tesirine(Cami,原为ADCT-301)单药或联合PD-1抑制剂在CD25阴性的同基因结肠癌模型(表现为表达CD25的Tregs肿瘤浸润)的抗肿瘤效果。数据显示Cami能够有效耗竭调节性T细胞( Tregs),并且对特定的实体瘤具有有效且持久的抗肿瘤活性。
Cami是一款靶向CD25的ADC药物,由CD25单抗HuMax-TAC装载吡咯苯二氮平(PBD)二聚体毒素弹头而成。Cami一旦与靶细胞(可以是表达CD25的肿瘤细胞,也可以是表达CD25的Tregs)结合,Cami就会被内化到细胞中,释放毒素以杀死目标细胞。
对于实体瘤来说,限制其进行免疫治疗的一大因素是免疫抑制性肿瘤微环境,其中Tregs起到了关键作用。靶向CD25的ADC药物消耗Tregs,诱导基于CD8+ T细胞杀伤作用的肿瘤免疫消除肿瘤。目前Cami正在进行一项针对晚期实体瘤的1b期临床试验、一项针对复发/难治性霍奇金淋巴瘤的2期临床试验以及一项针对非霍奇金淋巴瘤的1b期临床试验。
(信息来源:
https://jitc.bmj.com/content/8/2/e000860.altmetrics;
https://ir.adctherapeutics.com/press-releases/press-release-details/2020/ADC-Therapeutics-Announces-Publication-Highlighting-the-Potential-of-Camidanlumab-Tesirine-Cami-as-a-Novel-Immuno-oncology-Approach-for-Solid-Tumor-Cancers/default.aspx.)
勃林格殷格翰靶向TRAILR2/CDH17新型双特异性抗体治疗晚期胃肠道癌即将进入临床I期
9月10日,勃林格殷格翰(Boehringer Ingelheim)公司宣布其研发的靶向TRAILR2/CDH17双特异性抗体BI 905711治疗晚期胃肠道(GI)癌症患者的I期临床试验即将正式开展。
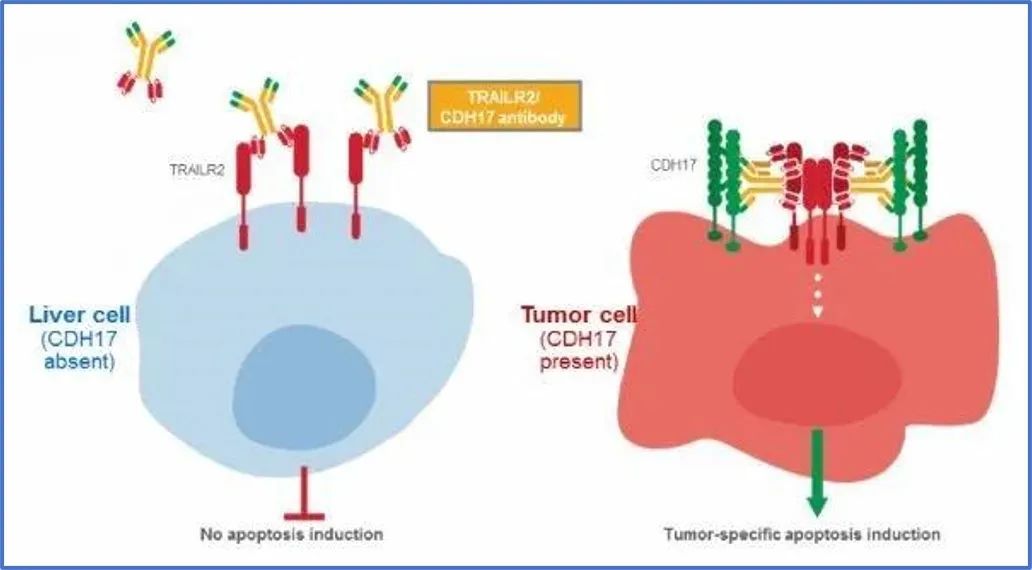
BI 905711是一款first-in-class新型抗体,是一种同时靶向识别促凋亡肿瘤坏死因子TNF相关凋亡诱导配体TRAILR2和锚钙粘着蛋白17(CDH17)的双特异性、四价治疗性抗体,通过激活肿瘤细胞的自我凋亡通路杀伤肿瘤细胞。目前晚期胃肠道恶性肿瘤缺少创新治疗选择,仍以副作用严重的化疗治疗为主;相对于只针对TRAILR2的治疗方法,该新型双特异性抗体治疗方法没有常见的肝脏毒性,可能为晚期胃肠道癌症患者提供创新性的无毒的治疗选择。
(信息来源:
https://www.biospace.com/article/releases/boehringer-ingelheim-advances-novel-bi-specific-trailr2-cdh17-antibody-to-phase-1-clinical-trial-for-patients-living-with-gastrointestinal-cancers/)
临床研究
9月7日,Nordic Nanovector公司在Blood Advances上发表了其靶向CD37抗体-放射性核素偶联疗法--Betalutin 治疗复发/难治性非霍奇金淋巴瘤的1/2a期临床积极结果。
结果显示:中位随访24.5个月时所有74位患者中,总体缓解率(ORR)为61%,包括30%的完全缓解(CR)。最常见的不良事件(AEs)为治疗后5至7周可逆的3/4级中性粒细胞减少症(31.6%)和血小板减少症(26.3%),最常见的非血液学不良事件为1/2级恶心(15.8%)。
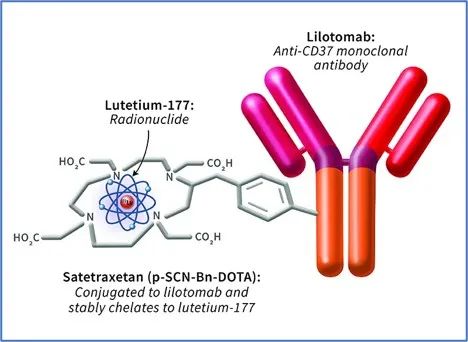
Betalutin又名lutetium lilotomab satetraxetan,为靶向CD37的抗体-放射性核素偶联疗法。Betalutin通过靶向肿瘤细胞表面的CD37蛋白,内化至肿瘤细胞中,使其细胞核长期暴露于核素的放射性辐射下,破坏肿瘤细胞DNA并导致死亡。这种新型靶向CD37的治疗手段为传统CD20抗体药物耐药的非霍奇金淋巴瘤患者提供了一种新的选择。
(信息来源:
https://ashpublications.org/bloodadvances/article/4/17/4091/463597/Phase-1-2a-study-of-177Lu-lilotomab-satetraxetan)
基础研究
9月9日,Nature分别发表了来自英国和美国两个团队的最新研究。这两份研究默契的共同揭示出TRIM37在细胞有丝分裂过程中的调控作用,以及PLK4抑制剂对于治疗TRIM37高表达肿瘤的潜力。
来自英国的科学家团队发现,一部分TRIM37高表达的癌细胞的细胞分裂对中心体有极高的依赖性。使用能够干扰中心粒(中心体的核心结构)形成的PLK4抑制剂药物可以使TRIM37蛋白高表达的癌细胞无法分裂,最终死亡。来自美国的科学家团队进一步阐明了TRIM37的作用机理。在“无中心体”的细胞内,当TRIM37水平较低时,PLK4会发生自组装,成为细胞分裂所需的微管组织中心,允许细胞进行分裂增殖;而当TRIM37水平较高时,会促进一种叫做CEP192的蛋白质的降解,这会抑制纺锤体的形成,从而抑制细胞的分裂。
在一些乳腺癌、神经胶质瘤中TRIM37高表达较为常见。这两项研究完整地阐明了TRIM37对细胞分裂的影响,也表明了PLK4抑制剂有望成为一类全新的抗癌药物。
(信息来源:
https://www.nature.com/articles/s41586-020-2690-1;
https://www.nature.com/articles/s41586-020-2710-1.)
NCB:PD-L1在介导肿瘤细胞焦亡和肿瘤坏死过程发挥关键作用
9月14日,Nature Cell Biology在线发表了来自美国德州大学洪明奇团队的最新研究。该研究第一次揭示了与巨噬细胞焦亡截然不同的肿瘤细胞的焦亡通路,并发现了PD-L1的非免疫检查点的功能,为后续的肿瘤治疗提供了重要的参考。
PD-L1参与的细胞焦亡过程包括PD-L1进入细胞核的过程和在TNF-alpha刺激下的焦亡过程。研究团队过筛选多种常见的肿瘤刺激物,发现缺氧环境可以诱导PD-L1分子进入肿瘤细胞核,并与磷酸化的Stat3作为复合物结合在GSDMC的启动子上共同介导了GSDMC而非GSDMD的表达。此时,使用TNF-alpha刺激,激活了肿瘤细胞中的Caspase-8,后者随之在D365位氨基酸处切割GSDMC,被释放的GSDMC氨基端自动整合于细胞膜上,形成的洞最终导致细胞涨破。
体内实验显示,抑制核PD-L1介导的细胞焦亡通路可以大大缓解肿瘤坏死症状并延长荷瘤小鼠的生存期。通过筛选临床常用的肿瘤化疗药物,发现抗生素类化疗药可以诱导三阴性乳腺癌MDA-MB-231细胞的焦亡,暗示了此类化疗药物在治疗三阴性乳腺癌时,细胞焦亡可能会对治疗效果产生一定影响。
(信息来源:
https://www.nature.com/articles/s41556-020-0575-z)
法规政策
9月11日,国家药品监督管理局药品审核中心发布了《药物相互作用研究技术指导原则(征求意见稿)》。本指导原则主要针对药代动力学的药物-药物相互作用(Drug-drug interaction,DDI)研究提供一般研究方法、常见评价指标和研究结果解读的通用指导,鼓励和引导企业在药物研发中合理制定研发策略,提高效率,规避风险,适时规范地开展药物相互作用研究。
指导原则对治疗蛋白药物的相互作用提出要求。治疗蛋白药物(therapeutic protein,TP)相互作用包括治疗蛋白药物与小分子药物之间的相互作用和治疗蛋白药物之间的相互作用两类。蛋白药物的相互作用应考虑的可能的机制包括但不限于:
(1) 促炎细胞因子相关机制:a)TP是促炎细胞因子时,细胞因子水平的变化可能会影响CYP表达以及CYP底物的活性和暴露程度;b)TP是细胞因子调节剂时:TP导致促炎细胞因子水平升高,此时应确定细胞因子水平升高的持续时间和程度;在细胞因子水平升高的情况下,TP调节促炎细胞因子,此时因疾病类型和疾病严重程度而异,导致CYP表达变化。
(2) 非促炎细胞因子相关机制:通常是已观察到或可预期的蛋白药物对其他药物有影响的情况,根据可能的作用机制来评估TP作为受变药或促变药。可能的机制包括但不限于:TP可改变合并用药物的药动学特性;影响TP靶标或靶点介导的药物处置;影响FcRn功能;TP与免疫抑制剂合并用药时受免疫原性影响的药代动力学改变。
(3) 抗体-药物结合物 (antibody-drug conjugate, ADC) :此时重要的是要了解ADC的小分子药物成分的全身暴露量。
(信息来源:
http://www.cde.org.cn/zdyz.do?method=largePage&id=948d1773f2d48da6)
版权声明
声明:以上资讯,仅供信息交流参考,不构成三优生物对外披露或投融资建议。










